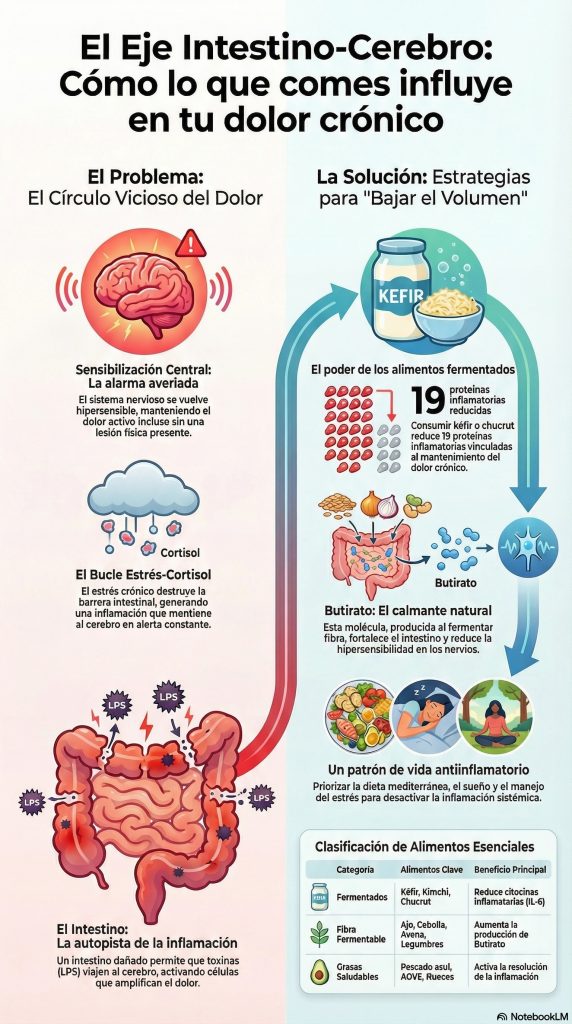
Y por qué eso importa si tienes dolor crónico
Si alguien te dice que lo que comes puede influir en cuánto te duele algo, puede que lo primero que pienses sea que es un consejo de curandero. No lo es. En los últimos quince años, la investigación científica ha ido construyendo una explicación bastante sólida de cómo el intestino, las bacterias que viven en él y lo que comemos cada día se comunican con el cerebro de una manera que afecta, entre otras cosas, a cómo percibimos el dolor. No hablamos de magia ni de bienestar indefinible. Hablamos de moléculas, receptores, nervios y citocinas. Y hablamos de algo que tiene consecuencias prácticas para cualquier persona que conviva con dolor crónico.
Este artículo explica qué es ese eje intestino-cerebro, cómo funciona en términos que no requieren un doctorado para entender, y qué puedes hacer —y qué no puedes esperar— con esa información.
Primero, lo básico: ¿qué es el dolor crónico realmente?
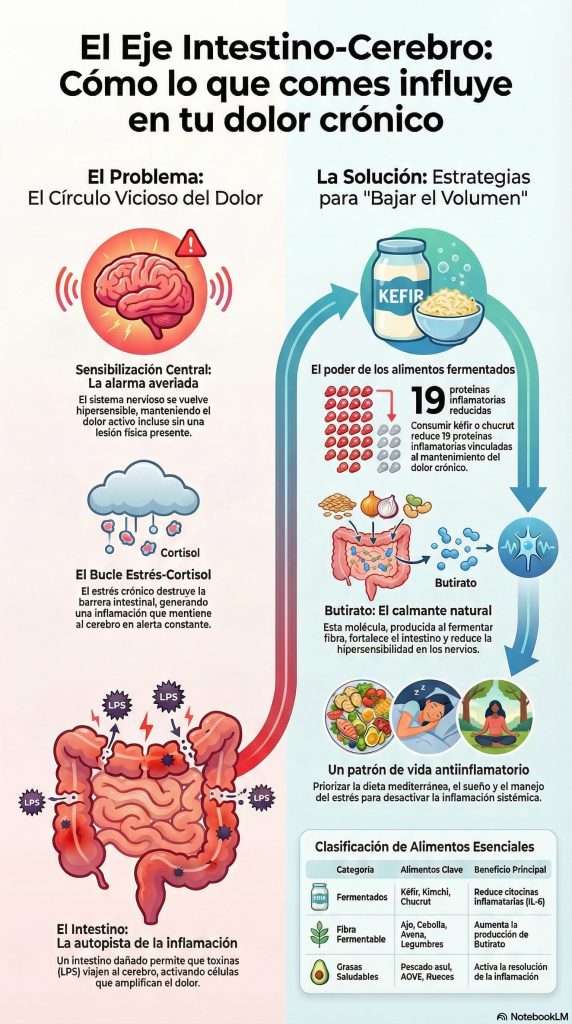
El dolor es una señal de alarma. Cuando te quemas un dedo, los nervios de la piel detectan el daño, mandan un mensaje a la médula espinal, que lo reenvía al cerebro, y el cerebro decide que hay una amenaza y genera la experiencia de dolor. Hasta aquí, todo tiene sentido evolutivo: el dolor te protege.
El problema empieza cuando ese sistema de alarma se queda encendido aunque no haya incendio. Eso es lo que ocurre en el dolor crónico: el sistema nervioso central —la médula espinal y el cerebro— se ha vuelto hipersensible. Los científicos llaman a esto sensibilización central. Es como si el volumen del sistema de alarma se hubiera subido tanto que ahora suena con cualquier cosa: un toque suave, el frío, la ropa rozando la piel.
Lo importante que hay que entender aquí es que en la sensibilización central el problema ya no está en el tejido dañado. Está en el cerebro y en la médula espinal, que han cambiado su forma de funcionar. El dolor es real —no está inventado, no es psicológico en el sentido peyorativo del término—, pero ya no refleja con fidelidad lo que ocurre en el cuerpo periférico.
¿Y qué tiene que ver con esto el intestino? Más de lo que nadie habría sospechado hace veinte años.
El intestino habla con el cerebro. Y mucho.
En tu intestino viven entre 38 y 100 billones de microorganismos, principalmente bacterias, que en conjunto se llaman microbiota intestinal. No son invasores: son residentes permanentes con los que hemos coevolucionado durante millones de años y de los que dependemos para muchas funciones esenciales, desde la digestión de ciertos nutrientes hasta la regulación del sistema inmune.
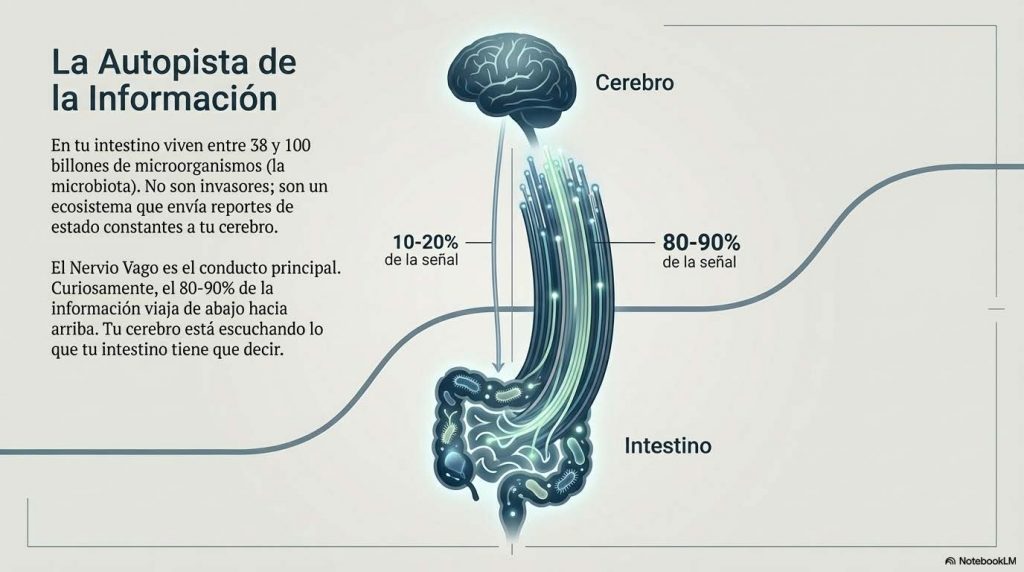
Lo que la investigación reciente ha puesto de manifiesto es que esta microbiota tiene una línea directa de comunicación con el cerebro a través de varios canales simultáneos. El más importante se llama nervio vago: un nervio largo que recorre el cuerpo desde el tronco encefálico hasta el abdomen y que actúa como autopista de información bidireccional. Lo curioso es que aproximadamente el 80-90% de esa información viaja hacia arriba, del intestino al cerebro, y no al revés. Tu intestino está mandando constantemente informes al cerebro sobre su estado, sobre lo que está ocurriendo en su interior, sobre qué bacterias están activas y qué moléculas están produciendo.
Hay otros canales: el sistema inmune —que conecta el intestino con el cerebro a través de citocinas, moléculas de señalización inflamatoria—, el sistema hormonal, y los propios metabolitos que producen las bacterias y que pueden llegar al cerebro por la sangre. Todo esto forma lo que se conoce como el eje microbiota-intestino-cerebro, y su disfunción está en el centro de un número cada vez mayor de enfermedades crónicas.
Inflamación: el fuego que nunca se apaga del todo
Para entender lo que sigue, hay que saber qué es la inflamación
La inflamación es la respuesta de defensa del sistema inmune ante una agresión: infección, daño tisular, cuerpo extraño. En su forma aguda es necesaria y útil: los tejidos se inflaman, combaten la amenaza y se recuperan. El problema es la inflamación crónica de bajo grado: un estado en el que el sistema inmune está permanentemente activado a un nivel bajo, sin que haya una amenaza real que lo justifique. Esta inflamación sostenida daña tejidos, acelera el envejecimiento y, como veremos, mantiene activos los circuitos del dolor.
Cuando la microbiota intestinal está en buen estado —diversa, rica en bacterias antiinflamatorias—, produce señales que ayudan a mantener el sistema inmune en equilibrio. Cuando la microbiota se deteriora —lo que se llama disbiosis—, ese equilibrio se rompe y el resultado es inflamación sistémica de bajo grado.
¿Cómo llega esa inflamación al cerebro? Por dos vías principales. La primera es directa: cuando la barrera intestinal se daña —algo que ocurre con la disbiosis, el estrés crónico y ciertas dietas—, unas moléculas bacterianas llamadas lipopolisacáridos o LPS se cuelan en la sangre. Cuando el LPS llega al cerebro activa unas células llamadas microglia, que son los macrófagos del sistema nervioso central, los guardias de seguridad del cerebro. La microglia activada libera citocinas inflamatorias —entre ellas TNF-α e IL-1β e IL-6— que alteran el funcionamiento de las sinapsis del dolor en la médula espinal.
La segunda vía es el nervio vago, que transmite las señales de estado del intestino directamente a regiones del cerebro como la amígdala —el centro de evaluación de amenazas— y el hipocampo. Un intestino inflamado manda señales de alarma al cerebro que este interpreta como una amenaza sostenida, y un cerebro que percibe amenaza sostenida mantiene el sistema del dolor en estado de alerta.
Investigadores de la Universidad de Stanford demostraron en un experimento publicado en la revista Cell en 2021 que una dieta alta en alimentos fermentados —kéfir, kimchi, chucrut, yogur con cultivos activos— reducía diecinueve proteínas inflamatorias en la sangre de los participantes, incluyendo la IL-6, una de las citocinas más directamente vinculadas al mantenimiento del dolor crónico. Este resultado, obtenido en adultos sanos, señala que la modificación dietética tiene efectos medibles sobre los marcadores del mismo proceso que alimenta la sensibilización central.
El butirato: la molécula que te importa conocer
Dentro de todo lo que produce la microbiota intestinal, hay una molécula que está recibiendo una atención científica extraordinaria en relación con el dolor y la inflamación cerebral. Se llama butirato y es un ácido graso de cadena corta que producen ciertas bacterias del colon cuando fermentan la fibra dietética que les llega.
El butirato hace varias cosas relevantes. Primero, fortalece la pared intestinal, reduciendo la permeabilidad que permite que el LPS se cuele a la sangre. Segundo, atraviesa la barrera hematoencefálica —la frontera entre la sangre y el cerebro— y actúa sobre la microglia, favoreciendo que pase de un estado inflamatorio a un estado de resolución. Tercero, actúa como regulador epigenético: modifica la expresión de genes en las neuronas, incluyendo genes relacionados con el factor de crecimiento neuronal BDNF, que es fundamental para la plasticidad y la recuperación neurológica.
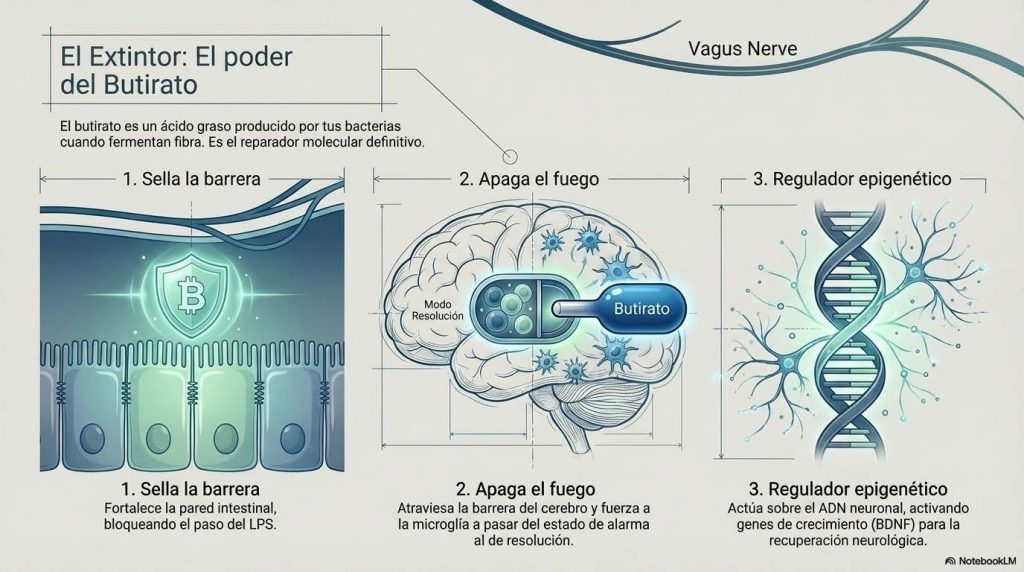
Experimentos en ratones con daño nervioso crónico han demostrado que la administración de butirato sódico durante dos semanas reduce significativamente la hipersensibilidad al dolor y los marcadores inflamatorios en el nervio afectado. Más interesante todavía: el butirato reduce la activación de la microglia en la médula espinal, actuando directamente sobre el mecanismo que mantiene la sensibilización central.
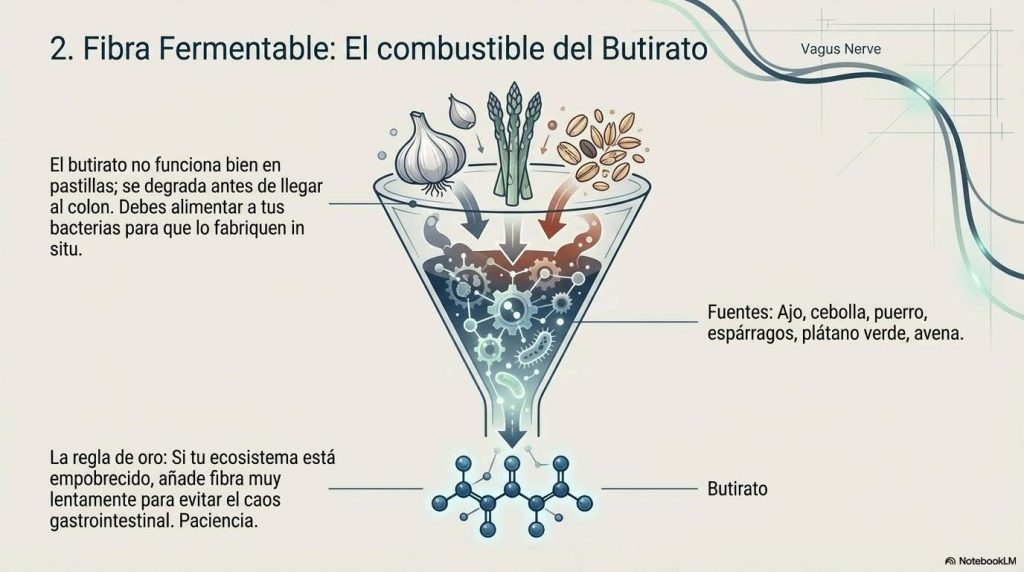
La pregunta práctica es: ¿cómo conseguimos más butirato? La respuesta es la fibra fermentable. El butirato no viene en cápsulas de forma efectiva —se degrada antes de llegar donde tiene que actuar—. Viene de que las bacterias adecuadas tengan suficiente sustrato para fermentar. Los alimentos más ricos en fibra fermentable son: ajo, cebolla, puerro, espárragos, alcachofa, plátano verde, avena, legumbres y achicoria. La variedad importa: distintos tipos de fibra alimentan distintas bacterias, y la diversidad bacteriana es en sí misma un marcador de salud.
El eje del estrés: por qué el círculo es vicioso
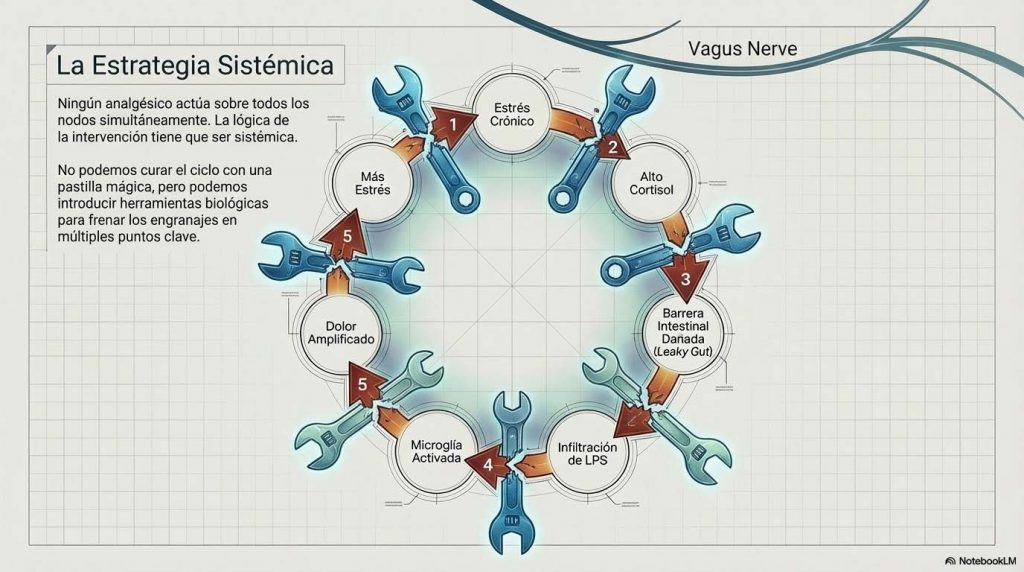
Hay un componente del sistema que convierte todo esto en especialmente difícil de romper: el eje del estrés, técnicamente conocido como eje hipotálamo-hipófisis-adrenal o eje HPA. Cuando vivimos bajo estrés crónico, este eje produce cortisol de forma sostenida. Y el cortisol tiene efectos directos sobre el intestino: deteriora la barrera intestinal, altera la composición de la microbiota favoreciendo bacterias proinflamatorias, y amplifica la producción de LPS.
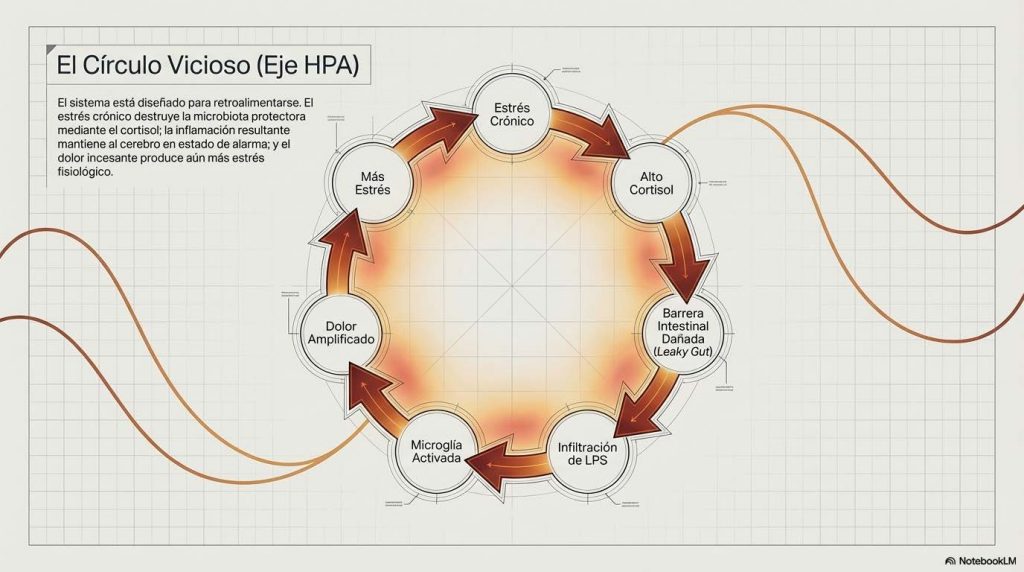
Al mismo tiempo, la disbiosis y la inflamación intestinal que produce el LPS activan el propio eje del estrés, produciendo más cortisol. El estrés destruye la microbiota protectora; la microbiota deteriorada genera más inflamación; la inflamación mantiene el cerebro en estado de alarma; el cerebro en alarma mantiene el dolor; el dolor crónico produce más estrés. Este es el círculo vicioso que explica por qué el dolor crónico es tan resistente a las intervenciones que solo atacan un punto del ciclo.
Ningún analgésico, por potente que sea, actúa sobre todos esos nodos simultáneamente. Un probiótico solo tampoco. Un cambio dietético solo tampoco. La lógica de la intervención tiene que ser sistémica, aunque cada acción individual sea modesta.
Lo que puedes hacer: evidencia real, sin exageraciones
1. Incorpora alimentos fermentados con regularidad
El estudio de Stanford que mencionamos antes no encontró este efecto con cápsulas de probióticos sino con alimentos fermentados reales: kéfir, chucrut, kimchi, yogur con cultivos activos, miso, tempeh. La razón probable es que los alimentos fermentados contienen una diversidad de microorganismos y de metabolitos que no replicamos con una cápsula de una cepa específica. Una o dos porciones diarias de alguno de estos alimentos es un punto de partida razonable. No es un tratamiento, pero sí es una intervención con respaldo experimental.
2. Cuida la fibra, pero con paciencia
La fibra fermentable es el combustible del butirato. Si tu microbiota está empobrecida —como ocurre en la mayoría de las personas en sociedades industrializadas—, aumentar la fibra de golpe puede generar molestias gastrointestinales porque el ecosistema bacteriano no está preparado para fermentarla. El enfoque más sostenible es el aumento gradual: añadir un alimento rico en fibra a la semana, dar tiempo al sistema para adaptarse. Ajo, cebolla, avena, legumbres, espárragos y plátano verde son buenas opciones.
3. Patrón mediterráneo como marco general
La dieta mediterránea —aceite de oliva virgen extra como grasa principal, pescado azul dos o tres veces por semana, legumbres, frutas y verduras de temporada, cereales integrales, frutos secos— tiene el mayor cuerpo de evidencia sobre reducción de inflamación sistémica de bajo grado entre todos los patrones dietéticos estudiados. Un metaanálisis de 22 ensayos clínicos aleatorizados publicado en 2022 confirmó que reduce consistentemente PCR, IL-6 y TNF-α, que son los mismos marcadores que aparecen elevados en muchos pacientes con dolor crónico. Los mecanismos son múltiples: los omega-3 del pescado azul son precursores de moléculas que activan activamente la resolución de la inflamación; los polifenoles del aceite de oliva, las bayas y las verduras modulan la expresión génica antiinflamatoria a través de la microbiota.
¿Y los omega-3 en cápsulas?
Una revisión sistemática de 41 ensayos clínicos con casi 4.000 pacientes, publicada en 2025, encontró que la suplementación con omega-3 producía una reducción significativa del dolor crónico, con mayor efecto a dosis moderadas y tratamientos de más de cuatro semanas. El efecto no es espectacular, pero es real y tiene mecanismo molecular documentado: los omega-3 EPA y DHA son precursores de mediadores de resolución que activan la transición de la microglia de un estado inflamatorio a uno antiinflamatorio. Como suplemento, son una opción razonable para quien no consume pescado azul con regularidad.
4. Reduce los ultraprocesados
Los alimentos ultraprocesados —bollería industrial, refrescos, snacks empaquetados, carnes procesadas— contienen aditivos como emulsionantes —carboximetilcelulosa, polisorbato 80— que en estudios en animales y algunos en humanos han mostrado capacidad para deteriorar la barrera intestinal y alterar la microbiota. Además, son pobres en fibra y ricos en grasas saturadas que activan directamente las vías inflamatorias NF-κB en el sistema inmune. Reducirlos no es la solución completa a nada, pero es uno de los cambios con mayor relación esfuerzo-beneficio en términos de inflamación sistémica.
5. El sueño y el estrés no son opcionales
Lo sabemos, ya nos lo han dicho, y sin embargo merece repetirse con respaldo científico: el sueño insuficiente altera la composición de la microbiota en días, no en meses. El estrés crónico deteriora la barrera intestinal directamente vía cortisol. Abordar el manejo del estrés —con las herramientas que funcionen para cada persona: actividad física, técnicas de regulación del sistema nervioso autónomo, apoyo psicológico— no es un complemento soft al tratamiento del dolor crónico. Es parte del mismo mecanismo biológico. El nervio vago que conecta el intestino con el cerebro también responde a la estimulación vagal —respiración lenta, actividad física moderada, contacto social— y su tono elevado se asocia con menor inflamación sistémica.

Lo que no puedes esperar: honestidad sobre los límites
Ninguna de estas intervenciones es una cura. La evidencia que conecta la microbiota con el dolor crónico en humanos es mecanicísticamente sólida pero clínicamente incompleta: la mayor parte de los estudios de intervención en dolor crónico son pequeños, de corta duración o realizados en modelos animales. Los mecanismos moleculares están descritos con precisión; la magnitud del efecto en pacientes con dolor crónico complejo —con su medicación, sus comorbilidades, su historia biográfica— está todavía siendo cuantificada.
Lo que sí puede decirse con honestidad es esto: la inflamación sistémica de bajo grado alimenta la sensibilización central que mantiene el dolor crónico. La microbiota intestinal regula en parte esa inflamación. La dieta modula la microbiota. Estos son eslabones de una cadena que la evidencia ha ido estableciendo con solidez creciente. Actuar sobre esa cadena —con coherencia, sin expectativas mágicas, como parte de una estrategia más amplia de manejo del dolor— es científicamente razonable y biológicamente justificado.
No sustituye a la fisioterapia, a la educación en neurociencia del dolor, al tratamiento farmacológico cuando está indicado, ni al apoyo psicológico. Se suma. Y en un sistema tan interconectado como el eje microbiota-intestino-cerebro-dolor, las sumas importan.
Una imagen para llevarte a casa
Imagina que el dolor crónico es un fuego que se mantiene encendido en tu sistema nervioso central. Hay muchas manos que lo alimentan: el estrés sostenido, el sueño insuficiente, el sedentarismo, la memoria emocional de experiencias dolorosas, y también —y esto es lo nuevo— una microbiota empobrecida que produce demasiado poco butirato y demasiado LPS, que activa una microglia que libera citocinas que mantienen los circuitos del dolor en estado de alerta.
Cambiar la dieta no es apagar el fuego de golpe. Es retirar una de las manos que lo alimentan. No la única, pero tampoco una mano irrelevante. Y tiene la ventaja de que es una de las pocas intervenciones que actúa simultáneamente sobre la inflamación, la microbiota, el sistema inmune y el sistema nervioso central, sin efectos adversos y con beneficios añadidos sobre la salud cardiovascular, metabólica e inmune.

El intestino habla con el cerebro constantemente. Merece la pena cuidar lo que le contamos.
Sobre este artículo
Las afirmaciones de este texto están respaldadas por investigación científica publicada en revistas con revisión por pares. No se ha incluido ningún dato sin referencia verificable. Las referencias principales son: Woolf CJ (Pain, 2011); Ji et al. (Anesthesiology, 2018); Wastyk et al. (Cell, 2021); Bravo et al. (PNAS, 2011); Dinan, Stanton & Cryan (Biological Psychiatry, 2013); y revisiones sistemáticas de Frontiers in Immunology (2024), Frontiers in Neuroscience (2025) y Advances in Nutrition (2022).
Maribel Pastor Orduña · www.maribelpastor.es · Abril 2026