El concepto, su origen y su correcta colocación científica

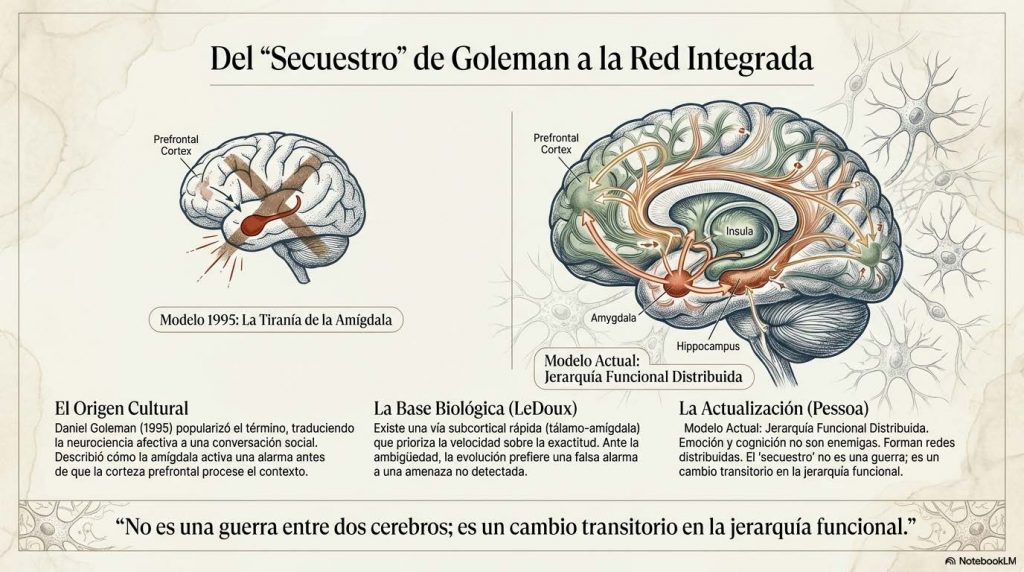
El término «secuestro amigdalar» entró en el lenguaje clínico y popular por una vía cultural, no experimental. Fue Daniel Goleman quien lo difundió en 1995 en *Emotional Intelligence*, un libro que marcó un punto de inflexión en la manera en que el mundo profesional hablaba de emoción, regulación y desempeño. Si vamos a usar este concepto con rigor, no basta con citarlo: hay que situarlo en su contexto histórico, científico y clínico.
Goleman no fue el descubridor de la arquitectura neurobiológica implicada en la respuesta de amenaza. Tampoco quien acuñó el término «inteligencia emocional» en el ámbito científico —fueron Peter Salovey y John Mayer, quienes en 1990 publicaron el primer artículo formal—.
Sin embargo, el impacto de Goleman fue decisivo porque integró investigación emergente en neurociencia afectiva con psicología aplicada; y la llevó a una conversación social amplia que trascendió los límites académicos. En otras palabras: no creó el fenómeno, pero lo tradujo y permitió que muchos clínicos empezaran a disponer de un lenguaje compartido para explicar algo que veían a diario en consulta pero que carecía de nombre accesible.
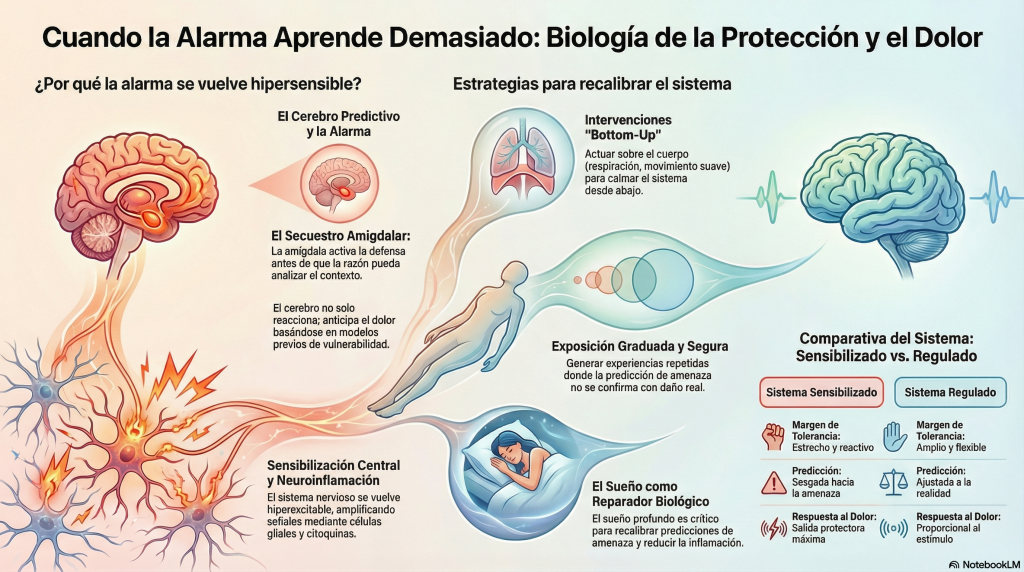
El «secuestro amigdalar» describe una situación en la que la amígdala cerebral, estructura límbica implicada en la detección de relevancia biológica y la asignación de gradación afectiva, activa una respuesta de alarma antes de que la corteza prefrontal haya podido elaborar un análisis detallado, integrado y flexible.
La metáfora es potente porque captura con precisión la vivencia subjetiva: la reacción precede al razonamiento. El cuerpo se moviliza antes de que la mente consciente pueda intervenir. La respiración se acelera, el corazón se dispara, los músculos se tensan y la atención se estrecha, todo ello antes de que exista una decisión deliberada.
Sin embargo, si nos quedamos únicamente en la metáfora, simplificamos en exceso un proceso que es mucho más complejo y matizado de lo que sugiere la imagen de un «secuestro».
La base experimental que sustenta la posibilidad de ese fenómeno procede de la neurociencia afectiva, especialmente de los trabajos de Joseph LeDoux en los años noventa, describió la existencia de rutas de procesamiento rápido en las que la información sensorial puede alcanzar la amígdala a través de una vía subcortical —tálamo-amígdala— antes de que la corteza procese el estímulo con la precisión y el detalle que caracterizan al procesamiento cortical (LeDoux, 1996).
Esta vía rápida, conocida como «ruta baja» o «low road», prioriza velocidad sobre exactitud. Evolutivamente tiene sentido: ante ambigüedad, es preferible activar una respuesta de defensa innecesaria —un falso positivo— que omitir una respuesta necesaria —un falso negativo que podría resultar letal—.
La investigación contemporánea ha demostrado de manera consistente que la emoción no reside en una estructura aislada ni se opone a la razón como si fueran entidades enfrentadas . Luiz Pessoa ha mostrado de forma convincente que emoción y cognición forman parte de redes distribuidas y profundamente integradas en las que la separación funcional es mucho más difusa de lo que sugiere la neuroanatomía clásica (Pessoa, 2017).
La amígdala interactúa de forma constante y bidireccional con la corteza prefrontal medial, la ínsula anterior, el hipocampo y otras regiones implicadas en la construcción de significado, la predicción corporal y la regulación autonómica. El llamado «secuestro» no es una guerra entre dos cerebros sino un cambio transitorio en la jerarquía funcional dentro de una red compleja, un desplazamiento temporal de la dominancia desde circuitos de evaluación contextual hacia circuitos de respuesta rápida.
La pregunta relevante no es si la amígdala se activa sino cuándo esa activación se vuelve desproporcionada, sostenida en el tiempo o predictivamente sesgada hacia la amenaza de manera que interfiere con la adaptación funcional.
Aquí es donde el concepto empieza a tocar terreno clínico real, especialmente en el contexto de condiciones crónicas donde la regulación del sistema de amenaza se encuentra alterada.
En consulta, la experiencia subjetiva de «perder el control» rara vez es un fenómeno aislado que aparece de la nada. Suele ocurrir en sistemas que ya están en estado de activación basal elevado. Sistemas que anticipan más de lo que esperan. Sistemas que han aprendido, a través de experiencias repetidas, que el cuerpo es vulnerable, que el entorno es impredecible, que la seguridad es frágil. Sistemas que, en suma, han aprendido vulnerabilidad. Y eso nos lleva inevitablemente al dolor persistente, un territorio en el que la alarma no solo aprende, sino que aprende demasiado.
Cuando el dolor se convierte en aprendizaje
El dolor crónico ha dejado de entenderse como simple prolongación temporal del daño tisular, como si la única diferencia entre dolor agudo y crónico fuera el calendario. Clifford Woolf describió la sensibilización central como un estado en el que el sistema nervioso central se vuelve hiperexcitable, amplificando la señal nociceptiva de manera que estímulos que en condiciones normales serían inocuos o levemente molestos generan respuestas de dolor intenso (Woolf, 2011). Esto implica reducción de umbrales de activación, expansión de campos receptivos neuronales y facilitación sináptica a través de mecanismos como la potenciación a largo plazo en las neuronas del asta dorsal de la médula espinal. No se trata de exageración psicológica, de «baja tolerancia» o de debilidad moral. Se trata de plasticidad neuronal real, medible, con correlatos biológicos específicos.
Posteriormente, Jo Nijs y colaboradores ampliaron este modelo al subrayar que en muchos pacientes con dolor persistente existe una alteración fundamental en el procesamiento central de amenaza y seguridad (Nijs et al., 2014, 2021). El sistema no solo transmite dolor de manera amplificada; lo interpreta en función de relevancia biológica, lo contextualiza dentro de una narrativa corporal, lo integra con experiencias previas. El dolor deja de ser únicamente señal ascendente y se convierte en output generado por una evaluación compleja que incluye memoria, expectativa, significado y contexto.
Si la evaluación de amenaza aumenta, la salida aumenta. Si el contexto se percibe como peligroso, el dolor se intensifica. Si la predicción apunta a vulnerabilidad, el sistema protege con mayor agresividad.
En este punto, el secuestro amigdalar deja de ser una anécdota emocional circunscrita a situaciones de estrés agudo y se convierte en pieza dentro de un sistema más amplio de priorización protectora que opera de manera crónica en condiciones de dolor persistente. La amígdala participa activamente en la asignación de relevancia a estímulos interoceptivos —señales que provienen del interior del cuerpo— y exteroceptivos —señales del entorno—. Cuando el sistema ha aprendido que determinados movimientos, contextos o sensaciones corporales preceden al dolor, la activación amigdalar puede adelantarse a la confirmación sensorial completa. La predicción pesa más que la señal. El sistema no espera a comprobar si realmente hay peligro; actúa basándose en la probabilidad aprendida de que lo haya.
Y aquí entra un elemento conceptual que no puede quedar fuera si queremos rigor: el cerebro no es solo reactivo; es fundamentalmente predictivo.
El cerebro no espera a recibir información completa; anticipa, predice, y solo procesa con detalle aquello que no se ajusta a la predicción. Si el sistema ha aprendido que el cuerpo es impredecible, frágil o vulnerable, asignará mayor precisión —mayor peso— a la señal de amenaza. Esa precisión determina cuánto influye una señal particular en la predicción final. Si la precisión atribuida a la amenaza es alta, cualquier señal ambigua se interpretará como confirmación de peligro. Esto no es pesimismo. Es aprendizaje. Es el resultado lógico de un sistema que ha extraído patrones de experiencias previas y los usa para navegar la incertidumbre.
He observado en mi práctica clínica —y he vivido en mi propia experiencia corporal— que lo que más desregula no es necesariamente la intensidad absoluta del dolor, sino su imprevisibilidad. Cuando el cuerpo puede cambiar sin aviso previo, cuando no existe patrón claro que permita anticipar o controlar los episodios, la anticipación se convierte en estrategia de supervivencia. El sistema aprende a ir por delante, a proteger antes de que llegue la confirmación. En este contexto, hablar de «control emocional» como si fuera cuestión de voluntad resulta superficial e incluso contraproducente. No se trata de voluntad. Se trata de estado basal del sistema nervioso. Y el estado tiene biología. No es metáfora. No es subjetividad pura. Tiene correlatos medibles, modificables, tratables.
Parte III — La conversación entre inmunidad y dolor
El sistema nervioso no funciona en aislamiento hermético. Funciona en diálogo constante, bidireccional y profundamente integrado con el sistema inmunitario. Y ese diálogo cambia de manera sustancial el umbral de la alarma. En los últimos años, la investigación en neuroinmunología ha mostrado de forma inequívoca que la microglía y los astrocitos no son simples células de soporte estructural o metabólico. Son participantes activos y dinámicos en la modulación de la excitabilidad neuronal. Cuando se activan —por infección, lesión tisular, estrés sostenido o inflamación sistémica crónica— liberan citoquinas proinflamatorias como interleucina-1β (IL-1β), interleucina-6 (IL-6) o factor de necrosis tumoral alfa (TNF-α) que alteran la transmisión sináptica, facilitan la señal nociceptiva y reducen los mecanismos endógenos de inhibición descendente del dolor (Ji et al., 2018).
A este fenómeno se le ha llamado en ocasiones «priming» glial o sensibilización glial. Un sistema primado responde con mayor intensidad y rapidez a estímulos posteriores. Desde fuera puede parecer desproporción, reacción exagerada o falta de resiliencia. Desde dentro es coherencia biológica: el sistema está operando de acuerdo con su estado actual, no de acuerdo con el estímulo aislado.
En dolor persistente, esta dimensión inmunológica es esencial y no puede ser ignorada. La nociplasticidad —dolor sostenido por alteraciones en el procesamiento central más que por daño tisular activo en la periferia— no puede comprenderse solo desde la plasticidad sináptica clásica. La plasticidad inmunológica también importa. La glía facilita la transmisión. Las citoquinas modulan la excitabilidad. El eje hipotálamo-hipófisis-adrenal participa en la regulación del estado inflamatorio. El sistema nervioso simpático interactúa con células inmunes. El nervio vago modula la respuesta inflamatoria periférica.
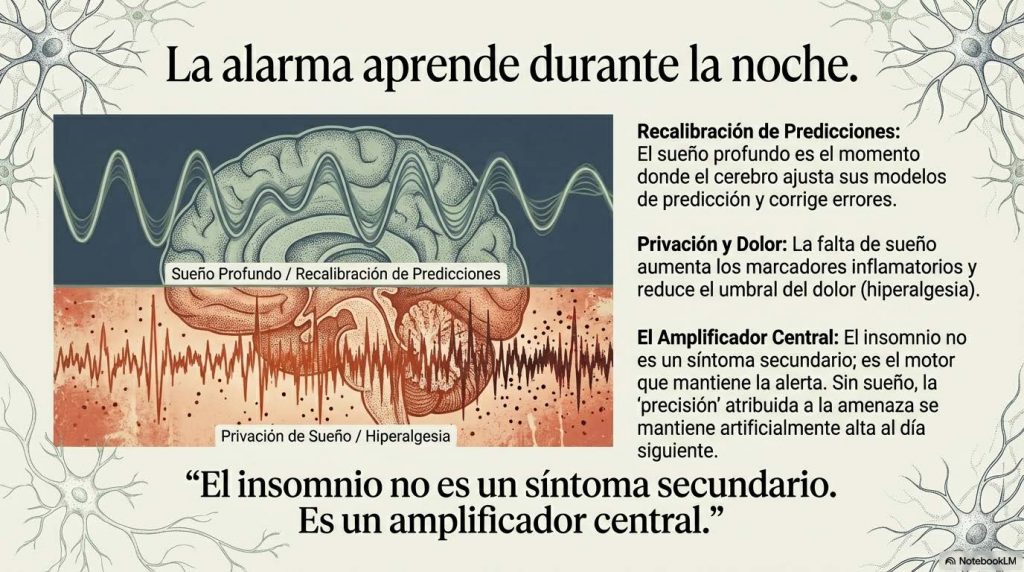
El sueño profundo, especialmente las fases de sueño de ondas lentas, regula la expresión génica, modula la liberación de citoquinas antiinflamatorias como IL-10, facilita la consolidación de memoria emocional y permite la recalibración de sistemas de evaluación de amenaza (Haack et al., 2007). Cuando el sueño se fragmenta de manera crónica —como ocurre con frecuencia en dolor persistente, donde el dolor interrumpe el sueño y la falta de sueño amplifica el dolor—, el sistema pierde una de sus principales ventanas de recuperación y regulación. La falta de sueño aumenta los niveles circulantes de marcadores inflamatorios. Reduce la tolerancia al dolor. Disminuye la capacidad de regulación emocional. Estrecha la ventana de tolerancia al estrés. No es casualidad que en muchas condiciones de dolor crónico la mejora del sueño sea uno de los predictores más consistentes de mejora funcional global.
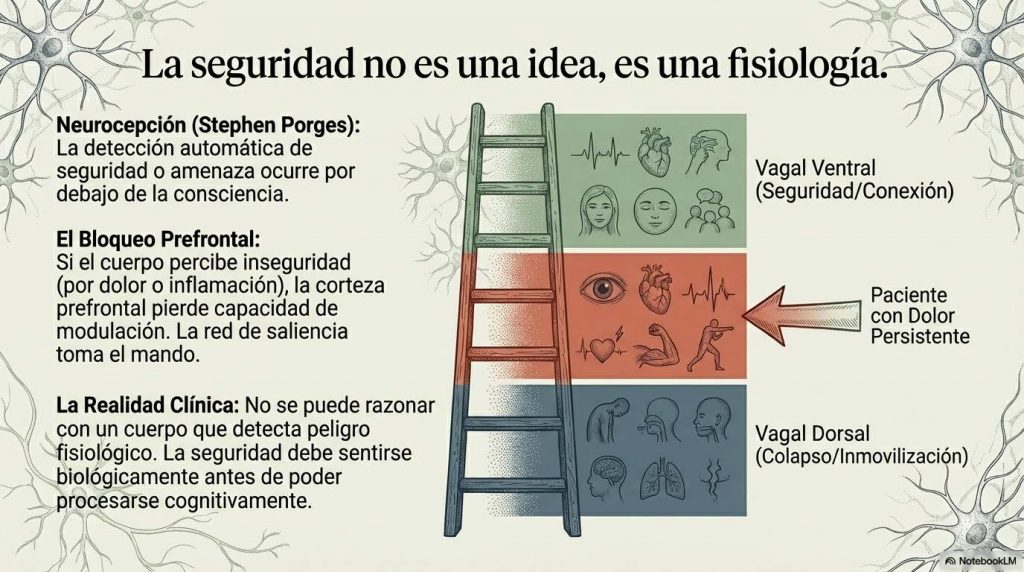
En dolor crónico, muchas personas oscilan entre activación simpática sostenida —que genera hipervigilancia, tensión muscular, fragmentación del sueño— y episodios de colapso dorsal —que se viven como fatiga abrumadora, desconexión, falta de motivación—. La ventana de regulación ventral se estrecha. El margen se reduce. La flexibilidad disminuye.
No es que el dolor sea «mental» en oposición a «real». Es que el dolor, cuando persiste, se convierte en parte de la arquitectura funcional del cerebro.
Parte IV — Predicción, aprendizaje y recalibración
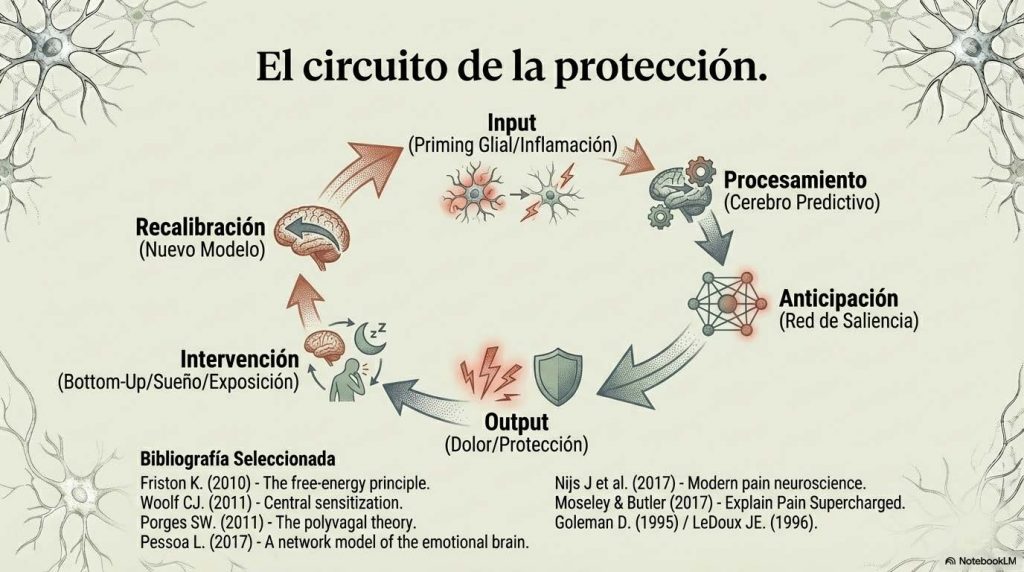
Cuando integramos todos estos elementos —sensibilización central, neuroinflamación, sueño fragmentado, desregulación autonómica, reorganización de redes cerebrales—, las respuestas que antes parecían desproporcionadas o inexplicables dejan de ser anomalías y pasan a ser consecuencias lógicas de un sistema que ha aprendido, que ha extraído patrones, que ha actualizado su modelo predictivo en función de experiencias repetidas. Karl Friston propuso que el cerebro funciona minimizando error de predicción (Friston, 2010). No espera pasivamente estímulos que procesar; genera hipótesis constantes sobre lo que va a ocurrir y ajusta esas hipótesis según la discrepancia entre lo esperado y lo recibido. Este proceso no es consciente. No es deliberado. Es la base misma de la percepción, la acción y la regulación corporal.
En este marco conceptual, la nocicepción no es simplemente una señal que asciende desde la periferia hacia el cerebro esperando ser interpretada. Es información que el sistema compara continuamente con su modelo interno de cómo debería ser el cuerpo. Si el modelo interno atribuye alta precisión a la amenaza —porque ha aprendido vulnerabilidad, imprevisibilidad, daño previo que no fue anticipado o protegido adecuadamente— la predicción tenderá a inclinarse hacia la protección incluso antes de que la señal sensorial esté completamente procesada en términos de detalle contextual.
La amígdala participa en esa ponderación de relevancia. Las redes de saliencia determinan qué señal merece prioridad de procesamiento. Cuando la precisión asignada a la amenaza es alta y el contexto se evalúa como inseguro, el sistema protege más rápido, con mayor intensidad y con menor umbral de activación.

Eso explica de manera coherente por qué en dolor persistente el movimiento puede generar miedo anticipatorio antes de generar daño real. Explica por qué una sensación corporal neutra o ambigua puede ser interpretada inmediatamente como preludio de crisis. Explica por qué la reacción emocional precede al análisis racional, por qué la persona puede «saber» intelectualmente que un movimiento es seguro pero sentir pánico al intentarlo.
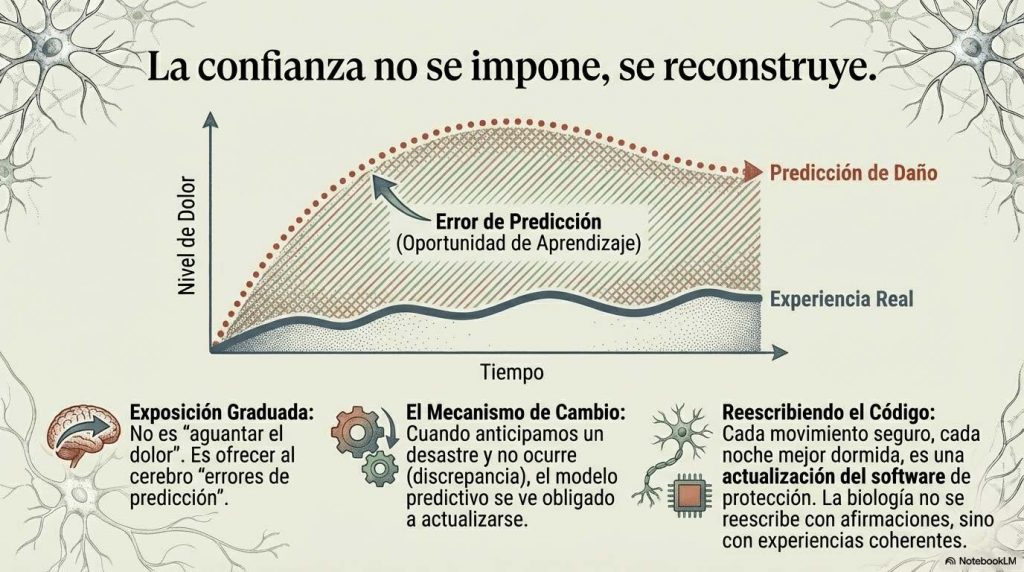
El cerebro no cambia por comprensión intelectual aislada. No basta con explicar la neurobiología del dolor, aunque esa educación es valiosa porque reduce culpa y ofrece contexto. El cerebro cambia por experiencia repetida que modifica la precisión asignada a sus predicciones.
Cuando un paciente con dolor persistente realiza un movimiento que anticipaba como devastador y la experiencia real, aunque no sea placentera, resulta tolerable y no genera el colapso esperado, se produce una discrepancia entre predicción y resultado. Esa discrepancia, si ocurre en un contexto suficientemente seguro y se repite con la frecuencia adecuada, permite ajustar el modelo. El sistema actualiza. La precisión atribuida a la amenaza disminuye ligeramente. El margen se amplía un poco.
Cuando alguien aprende a detectar el inicio de una activación autonómica —el cambio en la respiración, la tensión en el pecho, la aceleración del pulso— y logra modularla mediante herramientas como respiración diafragmática, movimiento suave, apoyo físico externo o conexión social segura, no está simplemente «controlando emociones» mediante esfuerzo de voluntad. Está ampliando el margen de regulación prefrontal sobre redes de saliencia. Está demostrando al sistema que existe capacidad de agencia. Está actualizando el modelo de vulnerabilidad hacia uno de mayor capacidad adaptativa.
En mi propia experiencia corporal, lo que más me ha transformado no ha sido entender la fisiología del dolor —aunque entenderla reduce significativamente la culpa y el miedo secundario—, sino experimentar repetidamente que no toda señal anticipada se cumple con la magnitud temida. Que el cuerpo puede atravesar un episodio difícil sin desmoronarse completamente. Que la alerta puede descender después de subir. Que la noche, a veces, puede conceder tregua. Que existe margen, aunque sea estrecho, para la regulación.
Y aquí vuelvo a Goleman, no como autoridad neurocientífica sino como puente cultural entre ciencia y práctica. El valor del «secuestro amigdalar» como concepto no está en convertir la amígdala en villana del sistema nervioso sino en permitir que alguien deje de interpretarse como defectuoso, débil o culpable cuando reacciona con intensidad e introducir la posibilidad de que la reacción sea un aprendizaje protector legítimo y no un fallo moral o caracterológico.
Pero el concepto debe usarse con rigor. No todo es secuestro amigdalar. No todo es trauma. No todo es inflamación. No todo es sensibilización central. La neurociencia contemporánea exige abandonar las dicotomías simplistas que dividen mente de cuerpo, emoción de cognición, biológico de psicológico. Emoción y cognición no están enfrentadas en una batalla interna; son aspectos de una red integrada que busca minimizar incertidumbre y maximizar supervivencia y bienestar.
En dolor persistente y enfermedad crónica, la intervención eficaz no consiste en convencer al paciente de que «no pasa nada», en negar la realidad de su experiencia o en minimizar su sufrimiento. Consiste en ofrecerle condiciones biológicas, contextuales y relacionales para que el sistema pueda comprobar, de manera gradual y segura, que a veces pasa menos de lo que anticipa. Que existe margen. Que la catástrofe predicha no siempre se materializa. Ampliar margen significa aumentar la ventana de tolerancia autonómica, mejorar la calidad y continuidad del sueño, modular la inflamación cuando es posible mediante intervenciones que pueden incluir ejercicio dosificado, alimentación antiinflamatoria, manejo del estrés o tratamiento farmacológico cuando esté indicado, dosificar el movimiento de manera que desafíe sin abrumar, reducir la culpa mediante educación y validación, ofrecer contexto seguro tanto físico como relacional, y permitir que el sistema experimente repetidamente que la predicción de catástrofe no siempre se confirma con la intensidad anticipada.
Y comprender esto no elimina el dolor ni borra la vulnerabilidad. No promete curación milagrosa ni elimina el sufrimiento. Pero cambia radicalmente la posición desde la que enfrentamos la experiencia.
Ya no se trata de luchar contra un cuerpo defectuoso que nos traiciona sin razón sino de acompañar a un sistema que ha aprendido, con coherencia biológica absoluta, a proteger. Un sistema que protege demasiado porque ha tenido razones para aprender que la protección es necesaria.
El camino no es lineal. Habrá retrocesos. Habrá días en los que el sistema vuelva al estado anterior porque algo —una noche mal dormida, un estresante inesperado, una infección menor— reactive el modelo antiguo. La biología de la protección no es enemiga. Es aliada que necesita información actualizada. Nuestra tarea, como clínicos y como personas que habitamos cuerpos complejos, es ofrecer esa información de manera que el sistema pueda integrarla. Con paciencia. Con rigor. Con compasión.
Implicaciones clínicas y perspectivas terapéuticas
La traducción de este marco conceptual a la práctica clínica requiere un cambio fundamental en cómo nos aproximamos al dolor persistente y a las condiciones crónicas que cursan con desregulación del sistema de amenaza. En primer lugar, es necesario abandonar el modelo de «corregir defectos» para adoptar un modelo de «actualizar aprendizajes».
Cuando un paciente llega a consulta con dolor crónico, con respuestas de ansiedad desproporcionadas o con patrones de evitación que limitan su vida, la tentación clínica es identificar qué está «mal» y tratar de eliminarlo. Pero si entendemos que el sistema ha aprendido a proteger de esa manera porque las circunstancias previas lo justificaban, el enfoque cambia radicalmente. Ya no buscamos eliminar una respuesta defectuosa, sino ofrecer experiencias que permitan al sistema actualizar su modelo de vulnerabilidad hacia uno más flexible y contextualizado.
Cuando vemos al paciente como portador de un aprendizaje legítimo, en lugar de como portador de una disfunción, la conversación cambia. La validación deja de ser un gesto empático superficial para convertirse en reconocimiento genuino de coherencia biológica. El paciente deja de ser alguien que «no sabe manejar el dolor» para convertirse en alguien cuyo sistema ha aprendido demasiado bien a anticipar amenaza. En segundo lugar, la intervención debe ser necesariamente multidimensional. No existe una única palanca que podamos mover para recalibrar un sistema complejo. Si la sensibilización central está sostenida por neuroinflamación, sueño fragmentado, desregulación autonómica, reorganización de redes cerebrales y modelos predictivos sesgados, la intervención efectiva debe tocar múltiples niveles.
La educación en neurociencia del dolor —lo que Moseley y Butler llaman «Explain Pain»— es componente fundamental, pero no suficiente. Explicar la biología del dolor reduce el miedo y la culpa, normaliza la experiencia y ofrece un marco de comprensión que puede ser profundamente liberador. Pero la comprensión intelectual no cambia, por sí sola, el modelo predictivo implícito. El sistema necesita experiencia, no solo información. El contexto relacional no puede ser ignorado. La teoría polivagal subraya que el sistema nervioso detecta seguridad no solo a través de evaluación cognitiva sino a través de señales implícitas del entorno social. La presencia de otro ser humano regulado puede co-regular. El juicio percibido puede intensificarla.
En mi práctica he observado que cuando un paciente siente que el clínico comprende genuinamente la lógica biológica de su experiencia, algo cambia en la consulta. Es que el sistema nervioso del paciente detecta, a nivel implícito, que no necesita defenderse de la incomprensión o del juicio. Importa si decimos «tu dolor es real» o «el dolor está en tu cabeza». Importa si validamos la coherencia del aprendizaje protector o si sugerimos que la respuesta es exagerada. El lenguaje no es neutro, ni el estimulo percibido, aunque algunos sostengan los contrario: activa o desactiva defensas.
Hay que preparar al paciente que la intervención no será lineal ni regular; ya que si anticipa progreso constante y encuentra oscilaciones, puede interpretarlo como evidencia de que «nada funciona», lo cual refuerza el modelo de vulnerabilidad.
También es importante reconocer que no todos los pacientes con dolor persistente tienen el mismo grado de sensibilización central, el mismo nivel de desregulación autonómica o la misma carga de neuroinflamación. La heterogeneidad del dolor crónico es enorme. Algunos pacientes tienen componente nociceptivo periférico significativo que requiere manejo específico.
La tarea clínica es identificar, en cada caso, qué mecanismos predominan y diseñar la intervención en consecuencia. No existe protocolo único. La personalización no es lujo; es necesidad.
Es imprescindible reconocer que el clínico también habita en un sistema nervioso que puede entrar en resonancia con el del paciente. Trabajar con dolor crónico, con trauma, con desregulación sostenida, puede activar nuestros propios sistemas de amenaza. Podemos experimentar frustración cuando el progreso es lento, impotencia cuando las intervenciones no funcionan como esperábamos, agotamiento cuando la carga emocional se acumula. Cuidar nuestra propia regulación no es autocuidado opcional. Es requisito profesional. Un clínico desregulado, por competente que sea técnicamente, transmite señales implícitas de inseguridad que el sistema nervioso del paciente detecta. La co-regulación funciona en ambas direcciones.
En resumen, la comprensión del «secuestro amigdalar» en el contexto del dolor persistente nos ofrece mucho más que una metáfora explicativa. Nos ofrece un marco integrado que conecta neurobiología, inmunología, fisiología del sueño, teoría de sistemas autonómicos, neurociencia predictiva y práctica clínica real; nos convoca, como profesionales y como seres humanos que también habitamos cuerpos vulnerables, a aproximarnos al sufrimiento con rigor científico y compasión genuina. A ofrecer comprensión sin simplificación. A acompañar sin rescatar. A sostener sin abrumar.
Ese es el trabajo. Riguroso, compasivo, paciente. Y profundamente humano.
Bibliografía
1. Goleman D. *Emotional intelligence: Why it can matter more than IQ*. New York: Bantam Books; 1995.
2. LeDoux JE. *The emotional brain: The mysterious underpinnings of emotional life*. New York: Simon & Schuster; 1996.
3. Pessoa L. A network model of the emotional brain. *Trends Cogn Sci*. 2017;21(5):357-371. doi:10.1016/j.tics.2017.03.002
4. Woolf CJ. Central sensitization: Implications for the diagnosis and treatment of pain. *Pain*. 2011;152(3 Suppl):S2-S15. doi:10.1016/j.pain.2010.09.030
5. Nijs J, Torres-Cueco R, van Wilgen CP, Girbés EL, Struyf F, Roussel N, et al. Applying modern pain neuroscience in clinical practice: Criteria for the classification of central sensitization pain. *Pain Physician*. 2014;17(5):447-457.
También relevante: Nijs J, Lahousse A, Kapreli E, et al. Nociplastic pain criteria or recognition of central sensitization? *Pain*. 2021;162(11):2621-2624.
6. Moseley GL, Butler DS. *Explain pain supercharged*. Adelaide: NOI Group Publications; 2017.
7. Friston K. The free-energy principle: A unified brain theory? *Nat Rev Neurosci*. 2010;11(2):127-138. doi:10.1038/nrn2787
8. Porges SW. *The polyvagal theory: Neurophysiological foundations of emotions, attachment, communication, and self-regulation*. New York: Norton; 2011.
9. Baliki MN, Mansour AR, Baria AT, Apkarian AV. Functional reorganization of the default mode network across chronic pain conditions. *PLoS One*. 2014;9(9):e106133.
Relacionado: Baliki MN, Geha PY, Apkarian AV. Beyond feeling: Chronic pain hurts the brain, disrupting the default-mode network. *J Neurosci*. 2008;28(6):1398-1403.
10. Haack M, Sanchez E, Mullington JM. Elevated inflammatory markers in response to prolonged sleep restriction are associated with increased pain experience. *Sleep*. 2007;30(9):1145-1152.
11. Ji RR, Nackley A, Huh Y, Terrando N, Maixner W. Neuroinflammation and central sensitization in chronic pain. *Anesthesiology*. 2018;129(2):343-366. doi:10.1097/ALN.0000000000002130
12. Salovey P, Mayer JD. Emotional intelligence. *Imagination, Cognition and Personality*. 1990;9(3):185-211.